![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
8 Cards in this Set
- Front
- Back
|
Ryhmä 2 |
Maa-alkalimetallit |
|
|
Mitkä alkuaineet |
beryllium (Be), magnesium (Mg), kalsium (Ca), strontium (Sr), barium (Ba) ja radium (Ra) |
|
|
Ulkoelektronien määrä |
2 |
|
|
Fysikaaliset ominaisuudet |
alhainen tiheys ja sulamispiste samankaltaisia alkalimetallien kanssa, mutta vähemmän metallisia. |
|
|
Kemialliset ominaisuudet |
esiintyvät yhdisteissä ionina M2+ esim. Ca2+ reagoivat happojen kanssa, mutta reaktiot ovat hitaampia kuin alkalimetalleilla. |
|
|
Tärkeitä yhdisteitä |
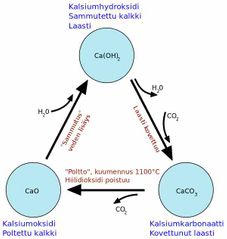
karbonaatit esim. CaCO3 oksidit esim. CaO hydroksidit esim. Ca(OH)2 |
|
|
Alkali- ja maa-alkalimetallien reaktioita |
Reaktiot veden kannsa 2 Na + 2 H2O —> 2 NaOH +H2 Ca + 2H2O —> Ca(OH)2 + H2 Suolahapon tai typpihapon kanssa Ca + 2HCl —> CaCl + H2 Ca + 2HNO3 —> Ca(NO3)2 (kalsiumnitraatti) + H2 Karbonaattien hajoaminen CaCO3 —> CaO + CO2 Reaktio halogeenin kanssa Ca + F2 —> CaF2
|
|
|
ERITYISIÄ REAKTIOITA |
Laastin kuivuminen Ca(OH)2 + CO2 —> CaCO3 + H2O Maantiesuolan CaCl2 valmistus (Solvayn prosessi) 2 NaCl + CaCO3 —> CaCl2 + Na2CO3 Metallioksidin reaktio vedessä CaO + H2O —> Ca(OH)2 Maa-alkalimetallin valmistus alumiinin avulla 3 BaO + 2 Al —> 3 Ba + Al2O3 |

