![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
18 Cards in this Set
- Front
- Back
- 3rd side (hint)
|
Kohlenhydrate (Allgemein) |
- organische Verbindungen aus Kohlenstoff, Wasserstoff, Sauerstoff - wichtigste Vertreter: Zuckermoleküle - Energielieferanten |
|
|
|
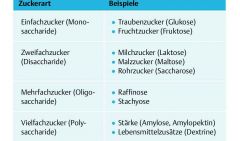
Kohlenhydrate (Einteilung) |
|
|
|
|
Monosaccharide (Einfachzucker) |
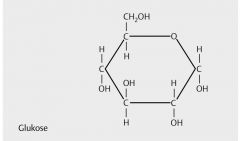
- bekannteste ist Glukose --> dient der Zelle als Energielieferant - einfache Zuckermoleküle bestehen aus einem ringförmigen Grundgerüst, je nach Art des Zuckers besitzt dieser Ring 5 oder 6 Ecken - Monosaccharide sind Bausteine für alle größeren Zuckermoleküle, Zweifachzucker entstehen, wenn Einfachzucker eine Verbindung eingehen |
|
|
|
Glukose (Formel + Struktur) |
|
|
|
|
Disaccharide (Zweifachzucker) |
- wenn eine Hydroxylgruppe (OH-Gruppe) eines Zuckers mit der eines anderen Zuckers reagiert - Beispiel Laktose (Milchzucker), bestehend aus Glukose oder Galaktose. --> bei diesen Reaktionen wird ein Wassermolekül abgespalten --> Kondensationsreaktion (= Reaktion bei der ein Wassermolekül freigesetzt wird) |
|
|
|
Oligosaccharide (Mehrfachzucker) |
Gehen Disaccharide eine weitere Verbindung mit einem Zuckermolekül ein, entstehen Trisaccharide und schließlich Oligosaccharide mit 3 - 10 Einheiten. |
|
|
|
Polysacchardie (Vielfachzucker) |
- riesige Makromoleküle mit bis zu Tausen Zuckerresten - Einteilung: - Homoglykane bestehen aus der gleichen Art Monosaccharide - Heteroglykane sind aus verschiedenen Zuckern zusammengesetzt - Glykonjugate sind Verbindungen aus Polysacchariden und Lipiden oder Proteinen |
Heteros halten Glee für Homo! |
|
|
Kohlenhydratstoffwechsel |
- Glukose wichtigster Energielieferant - Zellen "verbrennen" Glukose zu Kohlendioxid und Wasser, wenn ausreichend Sauerstoff vorhanden - Energiegewinnung verläuft in 4 Schritten: 1. Glykolyse 2. Oxidative Decarboxylierung 3. Zitratzyklus 4. Atmungskette |
|
|
|
Proteine (Allgemein) |
- wichtige Strukturen in Zellen und Gewebe - steuern Stoffwechselvorgänge und fungieren als Transporter und Speichersubstanzen |
|
|
|
Aminosäuren |
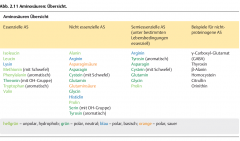
- der Mensch besteht zu etwa 15 % aus Proteinen, die wiederum aus AS bestehen --> diese AS nennt man proteinogene AS oder alpha - AS --> nicht-proteinogene AS sind in chemischen Botenstoffen wie Neurotransmittern oder Hormonen zu finden - Essenszielle AS: kann der Körper nicht selbst herstellen, mit Nahrung aufnehmen - Nicht-Essenzielle AS: 300 wurden in der Natur entdeckt, 12 kann der Mensch herstellen - im Zentrum einer AS immer ein Kohlenstoffatom (alpha-C-Atom), welches 4 Bindungen eingeht: --> mit COOH- bzw. Carboxylgruppe --> mit NH2- bzw. Aminogruppe --> mit einem Wasserstoffatom --> mit einem Rest, der sich von AS zu AS unterscheidet - AS sind Ampholyte, d.h. sie besitzen funktionelle Gruppen, die Basen- und Säureeingenschaften haben --> in einer sauren Lösung (ph-Wert < 7) wirkt die Aminogruppe (-NH2) als Base. Sie nimmt H+-Ionen auf und liegt dann als NH3 vor --> in einer basischen Lösung (ph-Wert > 7) fungiert die Carboxylgruppe (-COOH) als Säure. Sie gibt ein H+-Ion ab und liegt dann als COO- vor. - je nachdem, in welcher Position die Aminogruppe zum alpha-C-Atom der Carboxylgruppe steht, gehört sie einer anderen Aminosäurengruppe an: - alpha-Aminosäure: Carboxyl- und Aminogruppe befinden sich am selben C-Atom - beta-Aminosäure: die Aminogruppe befindet sich am 3. C-Atom - gamma-Aminosäure: die Aminogruppe befindet sich am 4. C-Atom
|
|
|
|
Grundstruktur der Aminosäuren |
BIlD |
|
|
|
Aminosäuren (Übersicht) |
|
Ich lalle mit Philipp tvt |
|
|
Einteilung der Proteine |
Motorproteine: Aktin und Myosin führen zur Kontraktion der Muskulatur, wodurch wir uns bewegen Strukturproteine: dienen als Gerüst, z.B. das Kollagen, das für Festigkeit und Flexibilität des Bindesgewebes verantwortlich ist, oder die Mikrofilamente Aktin, Tubulin und Keratin des Zytoskeletts Transportproteine: Transport von Stoffen, z.B. Hämoglobin, das den Sauerstoff transportiert Enyzme: bestehen aus Proteinen. Sie beschleunigen biochemische Reaktionen im Körper Speicherproteine: helfen Zellen, bestimmte Verbindungen zu speichern Signalproteine: sind Proteine, die endokrin, parakrin, synaptisch oder kontaktabhängig Signale weiterleiten Glykoproteine: sind Makromoleküle wie Antikörper, Plasmaproteine oder Zellmembranproteine. Sie bestehen aus kovalent aneinandergebundenen Mono, -Di, Oligo- oder Polysacchariden |
|
|
|
Proteine (Aufbau) |
- eine Kette von AS, die zusätzlich in unterschiedlichen Raumebenen strukturiert sind - Primärstruktur Abfolge der einzelnen AS innerhalb des Proteins - Sekundärstruktur Einzelnen AS gehen untereinander Wasserstoffbrückenbindungen ein --> AS-Kette verdrillt sich --> alpha-helix - Tertiärstruktur Setzt sich auch verschiedenen Sekundärstrukturen zsm. Charakterisiert die biochemische Funktion des Proteins. - Quartärstruktur Anordnung von zwei oder mehr Makromolekülen mit jeweiliger Tertiärstruktur, die durch Wasserstoffbrückenbindungen, Van-der- Waals Kräfte, oder elektrostatische Kräfte zusammengehalten werden |
|
|
|
Lipide und Fette (Allgemein) |
- haben mit etwa 9 kcal/g den höchsten Energiegehalt (Vgl. Kohlenhydrate 4,1 kcal/g) - Fett wasserfrei --> platzsparend - nicht geeignet als schneller Energielieferant --> langsamer Abbau - wichtiger Baustoff (Baufett) - mechanischer Schutz - Isolierung gegen Kälte - transportieren verschiedene Stoffe aus der Nahrung, z.B. die essenziellen und fettlöslichen Vitamine A, E, D, K |
fettlöslichen Vitamine: EDeKA |
|
|
Neutralfette (Tryglyzeride) |
- sind die größte Gruppe der Fette - bestehen aus Glyzerin (einem dreiwertigen Alkohol - 3 Hydroxylgruppen), der mit 3 Fettsäuren verknüpft ist --> Fettsäureschwänze sind langkettige Alkylgruppen (-CH2-CH2-etc.) --> je länger die Kette, desto weniger reaktiv sind Fettsäuren --> dadurch weisen sie Triglyzeride keine Polarität auf und sind somit nicht in Wasser löslich (-> Neutralfette) - abhängig davon wieviele Fettsäuren am Glyzerin verbunden sind, gibt es: - Triglyzeride (alle 3 möglichen Bindestellen (OH-Gruppen) des Glyzerins sind mit Fettsäuren besetzt - Diglyidezeride - Monoglyzeride |
|
|
|
Bildung eines Triglyzerids |
BILD |
|
|
|
Fettstruktur |
- je nachdem welche Art von FS mit Glyzerin verestert ist, unterscheidet man zwischen gesättigten und ungesättigten FS --> FS weist eine Doppelbindung zwischen den Kohlenstoffatomen (C-Atomen) der Fettsäurekette auf = einfach ungesättigte FS --> FS weist mehrere Doppelbindungen auf = mehrfach ungesättigte FS --> FS weist keine Doppelbindungen auf, alle C-Atome mit H-Atom abgesättigt = gesättigte FS Merken: - Je länger die FS sind und je mehr Einfachbindungen sie aufweisen, desto stabiler sind sie - Je mehr FS und je mehr Doppelbindungen sie beinhalten, desto instabiler sind sie |
|

