![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
69 Cards in this Set
- Front
- Back
|
Definer en konjugert base/syre |
En konjugert base dannes når en syre donerer et proton. Tilsvarende en konjugert syre dannes når en base mottar et proton. Kalles samlet for et konjugert par. |
|
|
Nevn noen amfoprotiske substanser, definer et zwitter ion. |
H2PO4(-), HCO3(-), H2O 2) Et zwitterion er en substans med en positiv og en negativ ladning. |
|
|
Hva kan en si om svake syrer/baser? |
Jo svakere syrer jo sterkere konjugert base formeres. Jo svakere base jo sterkere konjugert syre formeres. |
|
|
Hva kaller vi det når vi endrer 1 produkt eller 1 reagent og vi får en likevekt forandring? |
Mass-action effect. Massevirkningsloven |
|
|
Hva skjer i en kjemisk likevekt? |
Raten av produkt som dannes er lik raten av substrat som dannes. Konsentrasjonsforholdet er likt mellom reaktanter og produkt. |
|
|
Hvordan definerer vi bufferkapasiteten til en løsning? |
Defineres som antall mol av en sterk syre/base som får 1L buffer til å en 1-enhets forandring i PH. |
|
|
Hva forteller ionisk styrke? |
Ionisk styrke relaterer til styrken av det elektriske feltet i en løsning. Relaterer til det elektrostatiske potensialet. |
|

|
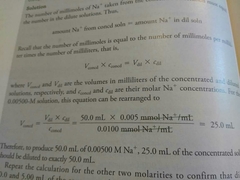
|
|

|
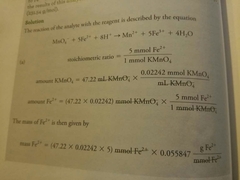
|
|

|

|
|

|

|
|
|
Hva er [H3O+] før endepunktet med en titrering HCl og NaOH? |

|
|
|
Hva er et ligand? |
En ione eller et molekyl som binder seg til et sentral metallatom. Ligandet må min. ha et par udelte elektroner. De fleste metallioner i vann løsning er som regel komplekser. Cu(NH3)4^2+ |
|
|
Hva kaller vi titreringer basert på komplekse formasjoner? Hva er et kjelat? |
Kompleksometriske titreringer. 2) Et kjelat blir dannet når et metall ion komplekserer med 2 eller flere donor grupper av et enkelt ligand og det formeres en 5 eller 6 heterosyklisk ring. |
|
|
Hva kalles et kompleks mellom et metallion og et syklisk organisk komponent? Hva står konstanten b for? |
Macrocycles. 2) summen av likevektskonstantene for kompleks formasjoner. b1,b2.......bn |
|
|
Hva hjelper konstanten b med? |
Gjør kalkuleringen enklere siden en ofte vet total konsentrasjonen, men det er ofte vanskelig å bestemme den frie ligand konsentrasjonen. |
|
|
Hvorfor foretrekker en ofte multidentante ligander i titreringer? |
Siden disse gir et mye skarpere ekvivalenspunkt. |
|
|
Hvorfor er løsninger med EDTA spesielt verdifulle som titranter? |
Siden disse danner komplekser med metallioner i et 1:1 forhold uansett ladningen av kationet. |
|
|
Hva ønsker vi å finne i en EDTA titrering? |
Kation konsentrasjonen som en funksjon mengden titrant EDTA lagt ved. |
|
|
Hva er forskjellen mellom svake og sterke elektrolytter? Eksempler |
Elektrolytter er stoffer som kan oppløses i vann og frigis til sine tilhørende kationer og anioner. Sterke elektrolytter dissosierer nesten fullstendig mens det motsatte gjelder for svake elektrolytter. Sterke elektrolytter inkluderer, sterke syrer/baser, salter. Svake syrer/baser er svake elektrolytter. |
|
|
Hva er amfiprotiske forbindelser? |
Et stoff som både kan donere og motta H+ ioner. |
|
|
Hva er forskjellen mellom en analytisk konsentrasjon og en likevektskonsentrasjon? |
Den analytiske konsentrasjonen er den totale antallet mol i en løsning uansett kjemiske tilstand. Likevektskonsentrasjon er den molare konsentrasjonen av en art i en løsning ved likevekt. |
|
|
Hvordan er forskjellen mellom andregradslikning og tilnærming relatert? |
Forskjellene avtar med større konsentrasjoner og avtagende Ka. |
|
|
Hva er autoprotolyse? |
Selvioniseringen av et stoff. Et molekyl oppfører seg som en brønsted syre og den andre som en brønsted base. |
|
|
Hva er massevirkningsloven ( Guldberg Waages lov, mass action effect)? |
En forandring i retningen av likevekten på grunn av addisjonen eller fjerningen av en art i likevekten. Eks A + B (⇆) AB. Legger til mer AB og likevekten forskyves mot reaktantene. |
|
|
Har faststoff en påvirkning på likevekten? |
Nei, konsentrasjonen tas som 1. Vann eksisterer i et så stort overskudd at det regnes som en konstant. |
|
|
Hva beskriver massebalanse? |
En massebalanse likning beskriver alle formene original komponenten kan ta i en løsning gjennom protonering eller deprotonering. |
|
|
Reaksjonslikninger og likevektsuttrykk for Ag3AsO4 ( sølv arsenat) |

|
|
|
Massebalanse og ladningsbalanse for sølv arsenat Ag3AsO4 |
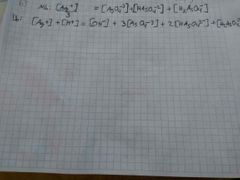
|
|
|
Hva er forskjellen mellom et kolloid og krystall bunnstoff? |
Kolloide bunnstoff har en diameter på mindre en 10^-4 cm. , Kolloider er ikke løselige for en gravimetrisk analyse på grunn av partikkelstørrelsen. Kolloider trenger en før behandling ( koagulering, tettbebyggelse (agglomeration), siden de ikke viser noen tendens til å komme sammen. |
|
|
Hva er forskjellen på en gravimetrisk bunnstoff metode og en gravimetrisk fordampningsmetode. ( Volitilization) |
1) Analytten blir gjort om til et lite løselig bunnstoff, som så filtreres, vaskes, konverteres til produkt med varmebehandling. 2) analytten fordampes, produktet blir samlet og veid, eller bestemmes indirekte fra tapet av massen. |
|
|
Hva er en primær standard? |
Primær standard er i kjemien et rent, fast stoff som benyttes direkte eller indirekte til å bestemme konsentrasjonen av en standardløsning |
|

|
Enzymhurtigheten er målt etter dannelsen produkt, I et typisk eksperiment er substratet i overskudd og hurtigheten måles direkte etter eller ved et senere tidspunkt. |
|
|
Hvordan oppnår enzymer sin maksimale hastighet? |
Ved en høy sunstrat konsentrasjonen er enzymet mettet og kan ikke katalysere raskere. |
|
|
Hvilken type titrering er en mohrs titrering? |
En type fellingstitrering hvor en utnytter reaksjonen mellom kloridioner og sølvioner. Får utfelling AgCl. Titranten er et lettløslig sølv eks AgNO3, indikator K2CrO4 gul ---- Ag2CrO4 (s) rødt/brunt). |
|
|
Hva slags type titrering er en volhard titrering? |
En fellingstitrering som er en tilbaketitrering. Det dannes først bunnstoff av AgCl fra eks AgNo3. Overskudd sølv blir så titrert med kScn eller naScn. Endepunktet registreres med Fe3+ ( dyp rød farge) |
|
|
Beskriv oksidasjon, redoksmiddel og en saltbro? |
1) Prosessen av tapet av elektroner ved en komponent i en redoks reaksjon. 2) En elektrondonor som reduserer den andre komponenten men blir seg selv oksidert. 3) En salt bro blir brukt til å tillate flyten av ladninger mellom to separate elektrolytiske løsninger uten at løsningene berører hverandre. |
|
|
Hva er liquid junction og nernst likning? |
1) Det er grensen hvor to forskjellige væsker med forskjellige komposisjoner møtes. 2) En likning som blir brukt til å relatere potensialet av halvcellen til standard elektrode potensialet. |
|
|
Beskriv forskjellen mellom oks. Og oks. middel? En elektrolytisk celle og galvanisk celle. |
1) Oksidasjon er tapet av elektroner, øker oks. tilstanden. Et oks. middel blir selv redusert og skaper oksidasjon av en annen komponent. 2) En elektrolytisk celle krever innsetting av energi, omgjør elektrisk energi til kjemisk energi. En Galvanisk celle skaper selv en elektrisk strøm, på grunn av forskjellen i det elektriske potensialet mellom de to cellene. Kjemisk energi til elektrisk energi. |
|
|
Hva er forskjellen på en katode av en elektrokjemisk celle og høyre hånd elektroden? En reversibel elektrokjemisk celle og en irreversibel elektrokjemisk celle. |
Katoden er hvor reduksjonen skjer i halvcellen. Den høyre hånd elektroden er koblet til den positive terminalen av et voltmeter. Den fungerer som en katode ved positiv volt og anode ved motsatt. 2) I en reversibel celle, ved voltforandring å skjer reaksjonen i motsatt retning. I en irreversibel reaksjon skjer en annen reaksjon ved når flyten av elektroner blir reversert. |
|
|
Forklar forskjellen mellom en standard elektrode potensial og et formelt potensial? |
1) Standard cellepotensial er forskjellen mellom potensialet i en halvcelle hvor reaktantene er i standard tilstander, bruker hydrogen elektrode. 2) Formel potensial har standard tilstand på reaktantene men det andre stoffet har ulik konsentrasjon. |
|
|
Hvorfor er det nødvendig å boble hydrogen gjennom elektrolytten i en hydrogen elektrode? |
For å holde aktiviteten av hydrogen konstant slik at det blir produsert et konstant potensial av elektroden. Hydrogen gass blir konstant boblet gjennom elektrolytten. |
|
|
Hvorfor er standard løsninger av reduktanter brukt mindre for titreringer enn standard løsninger av oksidanter? |
Hvis en bruker en standard løsning av reduktanter, så vil disse svært raskt oksidere med atmosfærisk oksygen. Derfor blir disse løsningene brukt sjeldnere. |
|
|
Hvorfor blir ikke Ce(+4) løsninger brukt for titreringer av reduktanter i en basisk løsning? Hvorfor er løsninger av KMnO4 og Na2S2O3 generelt lagret i mørke reagent flasker? |
Det blir utløst et bunmstoff av et cerium salt ved reaksjonen av ionet Ce(4+) og dem basiske løsningen. 2) Både KMnO4 og Na2S2O3 vil oksideres og katalyseres ved eksponering for lys som leder til deres nedbrytning. Derfor blir disse stoffene lagret i mørklagte flasker. |
|
|
Beskriv en indikator elektrode og en referanse elektrode? |
En elektrode ( noe som leder strøm) som responderer til en forandring i aktiviteten til en analytt i potensiometri ( måling av elektrisk potensial). 2) En halv celle som allerede har et kjent elektrisk potensial. Elektrode potensialet er uforandret ved konstant temperatur og er uavhengig av komposisjonen av analytten. |
|
|
Definer en elektrode av første type og en elektrode av andre type? |
1) Er en metallelektrode som responderer til en forandring i aktiviteten av kationet i reaksjonsblandingen. 2) En metall elektrode som responderer til forandringen av aktiviteten av anionet i reaksjonen. |
|
|
Hva er kilden av asymmetripotensial i membranelektroden? Grensepotensialet i membranelektroden? |
1) Forskjellen i den indre og ytre overflatemembranen av strukturen eller komposisjonen som leder til et asymmetri potensial. ( Kan være slitasje eller forurensing eks. ) 2) Kommer som følge av variasjonen av pHen av analyttkonsentrasjonen. Kan foresakes av opphopping av neg. ladning i de to membranoverflatene. |
|
|
Hva er kilden av et " junction potensial" i en glass/calomel elektrode? Potensialen av en krystallmembram elektrode brukt for å bestemme konsentrasjonen av F2 |
1) Potensial som som regel utvikles mellom prøveløsningen og den mettede KCl løsningen i saltbroen. Kan skyldes ladningsseperasjon. 2) Membranen av en F ion selektiv elektrode er satt sammen av en enkelt krystall LaF3 dopet med en liten mengde EuF2 for å øke ladningen. På grunn av den ulike løseligheten av LaF3 får en et ulikt potensial. |
|
|
Definer en milimol, titrering og et stokiometrisk forhold? |
1) Et mol er en substanse som imneholder like mange molekyler, atomer, elektroner ,ioner som 12 g Karbon. Milimol er 1/1000 del av dette. 2) Titrering er en kvantitativ kjemisk analyse. En standard løsning reageres med en ukjent konsentrasjon med målt mengde. Ved å bruke stokiometrisk forhold regner en seg fram til den ukjente konsentrasjonen. 3) I en balansert kjemisk likning er molforholdet lik et stokiometrisk forhold. |
|
|
Hva er en titreringserror? |
Vi må måle mengde reagent som gor et endepunkt. Denne verdien skal være lik en kalkulert teoretisk verdi for å nå endepunktet. Når disse to verdiene ikke stemmer så har vi en titreringserror. |
|
|
Hva er forskjellen på et ekvivalenspunkt og endepunkt av en titrering? Hva er forskjellen på en primær standard og en sekundær standard? |
1) Ved ekvivalenspunktet så er mengden titrant lagt til kjemisk ekvivalent med mengden analytt i prøven. Ved endepunktet er en kjemisk forandring observert som tilsier et ekvivalenspunkt. 2) En primær standard er en ren substans, som blir brukt som referanse for titreringsmetoder. En sekundær standard er en substans som sin konsentrasjon blir bestemt fra stoikiometri med sin reaksjon med en primær standard. |
|
|
Hvorfor viser den typiske base/syre indikatoren fargeforandring over et intervall av 2 ph enheter? |
Gitt en syrefarge HIn og en Indikator In er ikke øyet sensitiv til en fargeforandring når forholdet ( HIn/In)< 0.1 eller større enn 10. Forholdet fargeforandring er observerbar mellom 0.1-10). Mennesket kan skille mellom farger når indikatoren er 10x den andre formen, det er derfor naturlig å bruke en indikator ph omfang på pKa= +-1 |
|
|
Hvilke variabler kan foresake pH omfanget av en indikator to å forandre seg? |
Det som får pH verdien til å svinge for en indikator inkluderer 1) ionisk styrke, 2) tilstedeværelsen av organiske løsemidler 3) samling av kolloid partikler 4) Temperaturen av løsningen. |
|
|
Hvorfor er salpetersyre sjelden brukt for å forberede standard syreløsninger? |
På grunn av at det er et sterkt oks. middel. |
|
|
Kokepunktene av HCl og CO2 er nesten like ( -85 og -78). Forklar hvorfor CO2 kan bli fjernet fra en vanndig løsning med å koke midlertidig uten at noe HCl blir fjernet selv etter 1 time? |
Jo høyere damptrykket er jo lavere vil kokepunktet være. Dette gjelder ikke for CO2 eller HCl, de fordamper ikke ved den samme raten. En mulig forklaring er at CO2 ikke er sterkt bundet til H2O slik at vannet lett fordamper. Ved HCl ioniseres disse umiddelbart til H3O+, Cl- og HCl bli ikke tapt. |
|
|
Gi to grunner hvorfor KH(IO3)2 foretrekkes fremfor benzosyre som en primær standard for en 0.01 NaOH løsning. |
1) KHIO3 er en sterkere syre enn C7H6O2 som gjør det lett å bruke en indikator ( pH 4-10) 2) På grunn av høy molekylær masse av KHIO3 er det en mindre relativ vekterror som reagent. |
|
|
Forklar omstendigheten hvor konsentrasjonen av natrium hydroksid løsning vil være upåvirket ved absorpsjonen av karbondioksid? |
En standardisert løsning av NaOH reagerer hurtig med atmosfærisk karbondioksid og produserer natriumkarbonat i løsningen og også som faststoff. Det blir ingen error under titreringen ( med syreindikator) siden karbonatet vil reagere med hydronium ionene av syren. Resultatet er ingen systematisk error. |
|
|
Definer et ligand, kjelat, tetradentat kjelatmiddel og vann hardhet? |
1) Et molekyl eller ion som har minst et par fri elektroner til danne en koordinasjonsbinding med metall eller ion. 2) En kjelat har en sentralatom av metall bundet til et ligand. 3) En tetradentat kjelatmiddel har 4 par udelte elektroner plassert slik at de kan binde til et metallion. 4) Vann hardhet definerer kationer sin evne til å erstatte natrium eller kalium ioner såpe og deretter formere et uløselig produkt som skaper skummet i vasken. |
|
|
Definer adsorbsjon indikator, argentometrisk titrering, kondisjonel formasjonskonstant og EDTA forflyttning titrering. |
1) Adsorbsjon indikator brukes i en bunnfall titrering. Er en organisk komponent som absorberer og gor fargeforandring. 2) Argentometrisk titrering er en bunnfall titrering med sølv nitrat. 3) Definerer en stabilitetskonstant ved en gitt ph 4) Overskudd Mg eller zink kompleks løs. av EDTA blir lagt til analytten ( mer stabil) |
|
|
Beskriv 3 generelle metoder for EDTA titreringer. |
1) Potensiometrisk titrering- Bruker elektroder og endepunktet bestemt slik 2) Tilbaketitrering metoder- Komplekser kan bestemmes med det stabile EDTA 3) Forflyttning metoder - En analytt løsning danner et stabilt kompleks med overskudd EDTA + Zn, Mg ioner. Det skaper en forflyttningsreaksjon. |
|
|
Forklar hvordan trinnvis og totale formasjonskonstanter er relatert? |
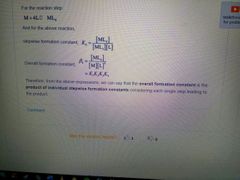
|
|
|
På hvilken måte er Fajans metode bedre enn Volhart metoden for titrering av kloridion? |
Fajans metode involverer en direkte titrering, slik at prosedyren er enkel og reproduserbar. Volhart metoden krever en indirekte metode som krever to standard løsninger og et filtreringstrinn. |
|
|
Hvorfor forandrer ladningen seg på bunnstoff partikler seg ved ekvivalenspunktet ved en titrering? |
Ved starten på en titrering er partiklene omgitt av et gitterioner med en ladning. Ved ekvivalenspunktet er det ikke lenger et overskudd av gitterioner. Partiklene blir nå omgitt av motsatt ladede gitterioner. |
|
|
Hvorfor eksisterer Fe som Fe(3+) under sure løsninger? |
Fordi en +3 ladning vil trekke mer på elektronene enn +2. H20 blir trukket mot det positive sentralatomet. [Fe(H2O)6]^3+ (aq) |
|
|
Beskriv forskjellen mellom en gravimetrisk bunnstoff og en gravimetrisk "volatilization" method? |
1) Dette involverer konversjonen av analytt til delvis løsbart bunnstoff, som så er filtrert og vasket, så konvertert til produkt. I gravimetrisk volatilization metode er analytten fordampet. Produktet blir så samlet og veid. Kan også bestemme masse produkt indirekte fra tapet av masse i prøven. |
|
|
En bunnstoff of kobunnstoff ( precipitation, coprecipitation)? |
Bunnstoff (precipitation) er en prosess der faststoff fasen er oppnådd og separert fra løsningen når en overskrider løselighetsproduktet. 2) Kobunnstoff ( Coprecipitation) er et fenomen av dannelsen av bunnstoff fra overflødig eller uønsket substanser sammen med det normale bunnstoffet. |
|
|
Hva er noen strukturelle kjennetegn ved et kjelatmiddel? |
Et kjelatmiddel vil fungere som et organisk bunnstoffgivende middel i en gravimetrisk analyse. Består av et ion eller molekyl ( ligand) som binder seg til et sentralatom. Kompleksene som blir formert av kjelatmiddelet vil generelt være ikke polart slik at det nesten ikle er løselig i vann. |
|
|
Hva er peptisering og hvordan unngåes dette? |
Definert som reverseringen av koagulering. Eks. er at en koagulert kolloid reverterer til sin originale spredning. Kan oppstå når elektrolytter forsvinner. |
|
|
Hva er en massebalanse likning? |
Et uttrykk som viser relasjonen mellom likevektsmolar konsentrasjonen av ulike sorter i en løsning til hverandre og til den molare analytiske konsentrasjonen av ulike løsninger. Enkelt fortalt beskriver likningen alle formene av originalstoffet kan ta i en løsning gjennom protonering og deprotonering. |

