![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
12 Cards in this Set
- Front
- Back
|
Que font les isomères? |
Les isomères causent l'absence de rotation possible autour d'une double liaison C=C. |
|
|
Combien et lesquels isomères existe t il? Que font ils? |
Il en existe 2: l'isomère Z, où les deux atomes d'hydrogène se trouvent du même côté de la double liaison; Ou l'isomère E, où ils se trouvent de part et d'autre. |
|
|
Représenter un isomère Z. |
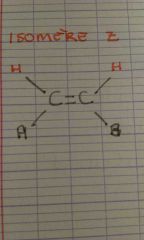
|
|
|
Représenter un isomère E. |
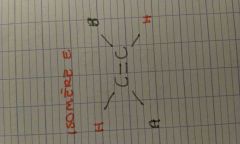
|
|
|
Représenter une molécule Tétraédrique. |

|
|
|
Représenter deux molécules linéaires. |

|
|
|
Représenter une molécule coudée |
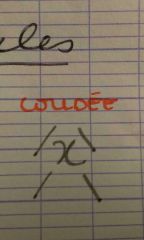
|
|
|
Représenter une molécule triangulaire. |
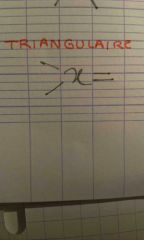
|
|
|
Représenter une molécule pyramidale. |

|
|
|
La représentation de Lewis contiens 3 liaisons chimiques. Lesquelles? |

|
|
|
Comment appelle-t-on les paires d'électrons externes ne participant pas à une liaison chimique? |
Doublets non liants. |
|
|
Ils existe deux regles concernant la dernière couche électronique d'une molécule. Lesquelles? En quoi consistent-elles? |
Règle du duet: les molécules possèdent deux électrons sur la couche externe. (Seulement 4 molécules sont concernés; H, Li, Be, He ) Règle de l'octet: les molécules possèdent huit électrons sur la couche externe. |

